Sie sparen
** auf Anfrage unter full-service@wer-gmbh.de **
Schnelle Gewissheit Made in Germany
• BfArM gelistet
• schnelle, zuverlässige Testergebnisse in 15 min.
• hohe Spezifität 99,9%, auch bei Mutationen
• hohe Sensitivität bei hoher Viruslast 97,56%
• einfaches Handling, hier zum Produktvideo
Die Anwendung des Antigen Schnelltests NADAL kann durch einen Abstrich durch die Nase und durch den Rachen erfolgen.
Keine Kreuzreaktivität mit humanpathogenen Coronaviren (wie hCoV-229E, -HKU1, -NL63 oder -OC43) beziehungsweise Influenza-Viren (wie Influenza A/B). Der NADAL® COVID-19-Antigen-Schnelltest ist ein chromatographischer Immunoassay im Lateral-Flow-Format zum qualitativen Nachweis von viralen SARS-CoV-2-Nukleoproteinen in humanen naso- und oropharyngealen Proben. Der Test ist als Hilfsmittel bei der Diagnose von Infektionen mit SARS-CoV-2 zugelassen.
Es ist zu beachten, dass die Konzentration der viralen Nukleoprotein-Antigene im Verlauf der Erkrankung schwankt und unter die Nachweisgrenze des Tests fallen kann. Eine mögliche Infektiosität der Testpersonen kann aufgrund negativer Testergebnisse nicht ausgeschlossen werden.
MHD: 10/2022
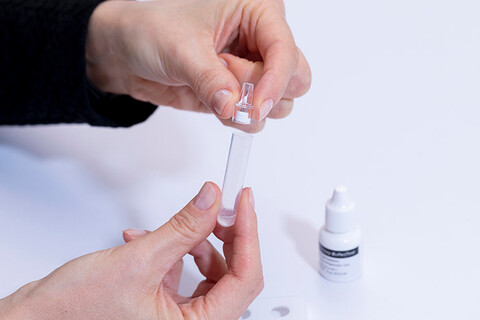
Anwendung:
Step 1
Step 2
Step 3
Step 4
Step 5
Der NADAL® COVID-19 Antigentest kann das veränderte Coronavirus, das in Großbritannien aufgetreten ist, ebenso zuverlässig nachweisen wie die aktuell bereits bekannten Varianten des Coronavirus.
Wie seit einigen Tagen bekannt ist, hat sich in Großbritannien eine neue Virusvariante des Coronavirus gebildet (genannt VUI-202012/01).
Dieses veränderte Virus weist auffällige Mutationen im Spike-Protein (S-Protein) auf, die einhergehen sollen mit einer erhöhten Ansteckungsgefahr. Nach aktuellem Stand können wir davon ausgehen, dass die Mutation des S-Proteins keine Auswirkungen auf die Nachweisbarkeit des Virus durch unseren NADAL® COVID-19 Antigen-Schnelltest hat.
Die nal von minden Schnelltests nutzen nicht das Spike-Protein (S-Protein) zum Nachweis des Virus im Probenmaterial, sondern das Nukleokapsid-Protein (N-Protein), das sich nicht verändert hat entsprechend den Informationen der Weltgesundheitsorganisation (WHO) und des European Centre for Disease Prevention and Control (ECDC).(1)
(1) https://www.ecdc.europa.eu/sites/default/files/documents/SARS-CoV-2-variant-multiple-spike-protein-mutations-United-Kingdom.pdf
https://www.who.int/csr/don/21-december-2020-sars-cov2-variant-united-kingdom/en/#:~:text=A%20total%20of%201108%20cases,cases%20in%20South%20East%20England.
Besonders geeignet für:
Pflegeeinrichtungen und Kliniken
Einreisekontrollen an Bahnhöfen, Raststätten und Flughäfen
Regelmäßige Tests von Betreuungspersonal und Mitarbeitern
Veranstaltungen, Messen und Versammlungen
Pharmazentralnummer: 16885532
Offizielle Bestätigung
Der NADAL® COVID-19 Ag Test erfüllt die durch das Paul-Ehrlich-Institut (PEI) in Abstimmung mit dem Robert-Koch Institut (RKI) festgelegte Kriterien für Antigen-Tests und wird auf der Whitelist des Bundesinstitutes für Arzneimittel und Medizinprodukte aufgeführt.
Bestandteile der Testverpackung:
NADAL® COVID-19 Ag je Testkassetten* (20 STk.) Gemäß 93/42/EWG mitgeliefertes zusätzliches Material:
*Enthält Konservierungsmittel Natriumazid: <0,1%
**Puffer enthält folgendes Konservierungsmittel:
Natriumazid: <0,1 mg/mL.
Gemäß Verordnung (EC) Nr. 1272/2008 CLP ist keine
Gefahrenkennzeichnung erforderlich. Die Konzentrationen
sind unterhalb der Freigrenzen.
Haltbarkeit und Lagerung
Die Test-Kits sollten bei 2-30°C bis zum angegebenen Verfallsdatum gelagert werden. Die Testkassetten sind bis zum auf dem Folienbeutel angegebenen Verfallsdatum stabil. Die Testkassette muss bis zum Gebrauch im verschlossenen Folienbeutel verbleiben. Frieren Sie die Test-Kits bitte nicht ein. Verwenden Sie die Tests nicht nach dem auf der Verpackung angegebenen Verfallsdatum. Es ist darauf zu achten, dass die Bestandteile des Test-Kits vor Kontamination geschützt sind. Verwenden Sie die Bestandteile des Test-Kits nicht, wenn es Anzeichen einer mikrobiellen Kontamination oder einer Ausfällung gibt. Biologische Kontaminationen von Dosiervorrichtungen, Behältern oder Reagenzien können zu falschen Ergebnissen führen
Warnung und Hinweis
Aktuell sind die Tests in Deutschland nur für den professionellen in-vitro-diagnostischen Gebrauch durch medizinisches Fachpersonal einzusetzen.
Klinische Nachweise
Der NADAL® COVID-19 Ag Test wurde mit klinischen Proben evaluiert, deren Status mittels RT-PCR bestätigt wurde (Ct-Bereich positiv: 20-37). Die Sensitivität wurde für den Bereich von hoher bis mittlerer Viruslast (Ct 20-30) und von hoher bis sehr geringer Viruslast (Ct 20-37) berechnet.
Diagnostische Sensitivität (Ct 20-30): 97,6% (93,1% – 99,2%)*
Gesamtübereinstimmung (Ct 20-30): 98,9% (96,9% – 99,6%)*
Diagnostische Spezifität: >99,9% (97,7% – 100%)*
Nachweisgrenze
Die Nachweisgrenze des NADAL® COVID-19 Ag Tests liegt bei 2 x 102,4 TCID50/mL und wurde mit einer SARS-CoV-2-Kontrolle mit einem bekannten Virustiter festgestellt. Die Nachweisgrenze des NADAL® COVID-19 Ag Tests liegt bei 0,4 ng/mL für rekombinante SARS-CoV-2-Nukleoproteine.